Los alquinos son moléculas orgánicos que se caracterizan por presentar en su estructura un triple enlace entre carbonos, como grupo funcional, por lo que también constituyen un tipo de hidrocarburo insaturado. Este triple enlace es el responsable de la reactividad y propiedades de estos compuestos, y en general se ajustan a la formula CnH2n-2.
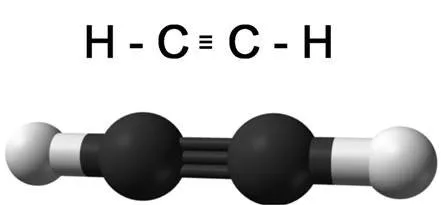
Estructura del acetileno. Fuente: wikipedia.com, dominio público.
Los alquinos son los hidrocarburos más insaturados, más que los alquenos, mientras que los alcanos son los saturados. Esto se debe a que el triple enlace sustituye mayor cantidad de átomos de hidrógeno con respecto a la fórmula del correspondiente alcano. Por ejemplo, la molécula H3C–CH3 al deshidrogenarse se obtiene el correspondiente alqueno, que sería el H2C=CH2, y si vuelve a eliminarse hidrógenos de la molécula se obtiene CH =CH, que sería el etino (o acetileno como también se le nombra). Como se habrán dado cuenta, en la medida que la molécula pierde átomos de hidrógeno los carbonos establecen enlaces adicionales entre ellos, ya que por su configuración electrónica, el carbono siempre tendera a satisfacer su estructura formando cuatro enlaces.
Respecto a la estructura de estos compuestos, donde hay un triple enlace la estructura de la molécula es lineal, en la siguiente imagen podemos observar la estructura de la molécula de acetileno, el alquino más sencillo de la familia.
La estructura de los alcanos se representa con un zigzag debido a los 109º de separación que se forma entre sus enlaces sencillos producto de la hibridación sp3 de los átomos de carbono, mientras que en los alquenos, sus carbonos experimentan una hibridación sp2, lo que conduce a la formación de un plano trigonal, ahora bien, en los alquinos la hibridación de los átomos de carbono es sp, lo que quiere decir que son en partes iguales carácter s y p, la distancia que separa los enlaces en los alquinos es de 180º , por esta razón el triple enlace en la molécula tiene una geometría lineal.
En comparación, el enlace triple entre carbonos en los hidrocarburos es mucho más fuerte, sin embargo esto requiere de mayor energía; por lo que un alcano puede convertirse en un alqueno, y este en un alquino, pero con reacciones a temperaturas más elevadas uno respecto al otro.
Una consecuencia del estado energético de estos compuestos, al romper el enlace se desprende una gran cantidad de energía que se manifiesta en forma de calor. Este hecho es observado, por ejemplo, cuando al quemar acetileno se produce tanto calor que se utiliza para fundir metales.

Llama de acetileno. Fuente: pixabay.com, domnio público.
Nomenclatura
Así como los alcanos y los alquenos, los alquinos se nombran mediante un conjunto de reglas establecidas por la IUPAC. Y siguen reglas similares, en el caso de los alquinos se nombran igual que el alcano con el mismo número de átomos de carbono, pero utilizando el sufijo –ino en lugar de –ano. Por ejemplo, si el H3C–CH3 es el etano, el H2C=CH2 es el eteno, y el CHΞCH sería el etino.
En general se siguen las siguientes reglas:
- Se determina cual es la cadena de carbono más larga que incluya ambos carbonos del triple enlace.
- Se numera la cadena más larga comenzando en el extremo más cercano al triple enlace.
- Después de numerar la cadena más larga con el número más bajo asignado al doble enlace, se identifican cada uno de los sustituyentes en su carbono correspondiente.
- Para escribir el nombre de la molécula, se ordenan los sustituyentes en orden alfabético. Cuando hay más de uno del mismo sustituyente, se usan los prefijos di, tri y tetra para identificarlos.
ejemplo
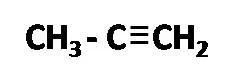
Propino
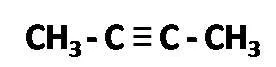
2-butino
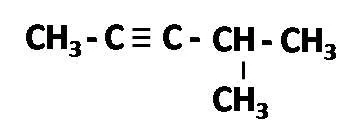
4-metil-2-pentino
Si está presente el grupo funcional del alcohol en la cadena, se numera la cadena comenzando por el extremo más cercano a él, ya que este grupo toma prioridad sobre el triple enlace.
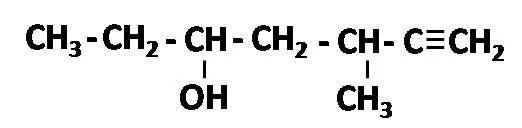
5-metil-6-heptin-3-ol
Cuando estén presentes dos triples enlaces en la cadena, determinamos cual es la cadena más larga que contiene a ambos triples enlaces. Se enumera la cadena empezando por el extremo más cercano al primer triple enlace, por ejemplo:
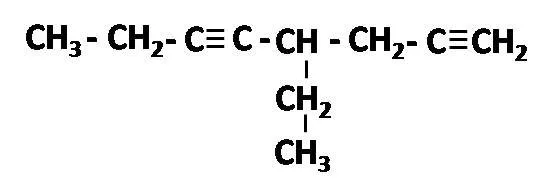
4-etil-1,5octadiino
Propiedades
Polaridad
Aunque los tres tipos de hidrocarburos (alcanos, alquenos y alquinos) son moléculas apolares, la electronegatividad de los carbonos del doble y triple enlaces es mayor que la de los carbonos simples. Por ello, los carbonos adyacentes al triple enlace, por efecto inductivo, les ceden densidad electrónica, como producto, donde este localizado el triple enlace habrá mayor densidad electrónica que en el resto de la estructura de la molécula, lo que origina un pequeño momento dipolar que les permite a las moléculas de estos compuestos establecer interacciones de tipo dipolo-dipolo, aunque sean muy débiles.
Puntos de ebullición y fusión
Gracias a esta pequeña interacción intermolecular por fuerzas dipolo-dipolo, los alquinos presentan puntos de ebullición y fusión más altos comparados con los alquenos con la misma cantidad de átomos de carbono.
Solubilidad
Por su polaridad, aunque pequeña, son menos insolubles en agua que los hidrocarburos menos insaturados. Y bastante solubles en solventes apolares.
Acidez
Otro efecto de esta débil polaridad, es que los alquinos sean especies más ácidas que los otros tipos de hidrocarburos, un poco más que los alquenos y mucho más que los alcanos. Sin embargo, su acidez es muy poca s se les compara con otros compuestos orgánicos propiamente ácidos, como los ácidos carboxílicos.
Aplicaciones
El más conocido de los alquinos por sus amplias aplicaciones también es el más sencillo de esta familia, el acetileno o etino. A partir de este hidrocarburo insaturado se pueden sintetizar otros compuestos orgánicos, mediante reacciones de oxidación se puede obtener etanol, etanal, ácido acético entre otros. También se usa para preparar material de partida para muchos polímeros útiles. Por ejemplo, el cloruro de vinilo es el material de partida para el PVC.

Tubos de PVC. Fuente: publicdomainpictures.net, dominio público.
También es conocido su uso para producir la llama de oxi-acetileno utilizada en el corte y soldadura.

Corte con soplete de acetileno. Fuente: pxhere.com, dominio público.
Los alquinos se encuentran en algunos productos farmacéuticos, incluido el anticonceptivo noretynodrel. Un triple enlace carbono-carbono también está presente en medicamentos comercializados como el antirretroviral Efavirenz y el antifúngico Terbinafine.
En la naturaleza también se encuentran en numerosas plantas, y se han aislado de estas fuentes, resultando altamente bioreactivos, por ejemplo como nematocidas.
Referencias
Chemistry Libre Texts. Alkynes
Wikipedia.com. Alkyne.
Libreria Británica. Alkyne.
Posted from my blog with SteemPress : https://moronej.000webhostapp.com/2019/03/alquinos